Iod là gì? Iod (I) hóa trị mấy? Tổng hợp đầy đủ kiến thức về I-ốt
Iod là gì? Iod (I) hóa trị mấy? Có rất nhiều em đã gửi thắc mắc về nguyên tố Iod trong bảng tuần hoàn hóa học. Bài viết này, Admin sẽ giúp các em trả lời, đồng thời có những kiến thức bổ ích nhất về nguyên tố I-ốt này. Bắt đầu bài viết để tăng cường hiểu biết của bản thân các em nhé!
Iod là gì?
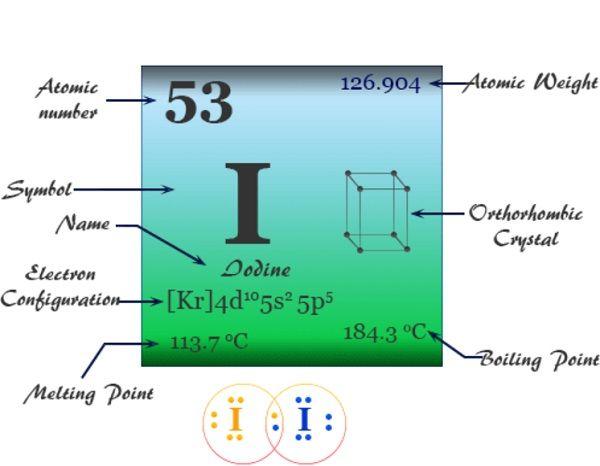
Iod hay Iodine là một nguyên tố hóa học với tên gọi bắt nguồn từ tiếng Hy Lạp là Iodes có nghĩa là “Tím”. Trong tiếng Việt, chúng ta vẫn thường gọi nguyên tố này là I-ốt với ký hiệu hóa học là I. Trong bảng tuần hoàn hóa học, Iod có số hiệu nguyên tử là 53, thuộc nhóm VIIA, chu kỳ 5 với khối lượng nguyên tử lag 126,9 đvC.
Bạn đang xem: Iod là gì? Iod (I) hóa trị mấy? Tổng hợp đầy đủ kiến thức về I-ốt

Iod là gì?
Iod (I) là một nguyên tố vi lượng rất cần thiết với sự sống của nhiều loài sinh vật khác nhau. Về mặt hóa học, nguyên tố này hoạt động ít trong nhóm các nguyên tố Halogen. Nó có độ âm điện thấp khoảng 2.66 theo thang đo Pauling.
Iod được sử dụng rộng rãi trong các ứng dụng y tế, bao gồm điều trị các rối loạn tuyến giáp và là thành phần chính của các chất tẩy khử và chất diệt khuẩn. Ngoài ra, Iod (I) cũng được sử dụng trong công nghiệp hóa chất, sản xuất chất tẩy, phân bón và các hợp chất hữu cơ.
Iod (I) hóa trị mấy?
Với số hiệu nguyên tử lag 53, nguyên tố I-ốt có cấu hình electron đầy đủ là: 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5. Vì lớp ngoài cùng có 5e nên Iod thường có xu hướng nhận thêm 1e trong hợp chất, do đó Iod (I) có hóa trị phổ biến nhất là -1. Tuy nhiên, Iod cũng có thể có các hóa trị khác như +1, +3, +5 và +7 trong một số hợp chất của nó.

Cấu hình e của I-ốt
I-ốt có mấy đồng vị?
I-ốt là nguyên tố có đến 37 đồng vị, trong đó:
- Chỉ có đồng vị I127 là bền
- Đồng vị I131 là đồng vị phóng xạ và nó phát ra hạt Beta với chu kỳ bán phân rã là 8,0207 ngày. I131 được đưa vào ứng dụng trong điều trị ung thư và các bệnh có liên quan đến tuyến giáp ở người.
- Còn đồng vị I123 cũng là đồng vị phóng xạ, nhưng nó được đưa vào ứng dụng trong chụp ảnh tuyến giáp và đánh giá trị liệu đối với bệnh Grave.
- Đồng vị I129 có chú kỳ bán phân rã là 15,7 triệu năm và nó có khả năng bán phá hạt nhân Xe129 bởi tia vũ trụ khi đi vào khí quyển Trái Đất.
Việc xử lý nhiên liệu hạt nhân và thử nghiệm vũ khí hạt nhân đã tạo ra lượng lớn I129 vượt trội so với tự nhiên. Đồng vị I129 được sử dụng trong nghiên cứu mưa sau vụ tai nạn Chernobyl và cũng có thể được sử dụng để phát hiện dấu vết chất thải hạt nhân trong mạch nước ngầm. Tiếp xúc với I129 có thể gây nguy cơ ung thư tuyến giáp, và người sống gần các khu vực phản ứng phân hạch thường được khuyến cáo sử dụng viên Iod (I) để ngăn ngừa hấp thụ I129.
I129 có tính chất tương tự với Cl36, là một halogen hòa tan, ít hoạt động hóa học và tồn tại dưới dạng ion không hấp thụ. Mật độ 129I được đo bằng tỷ lệ I129 so với tổng iod, và nó tồn tại trong tự nhiên ở mức rất thấp. Đồng vị I129 có chu kỳ bán rã dài hơn và có sự hiện diện trong sinh vật dưới dạng ion với nhiều hành vi hóa học khác nhau. Nó dễ dàng nhập vào sinh quyển và có thể được tìm thấy trong cây cỏ, đất, sữa và mô sinh học.
Lịch sử phát hiện và nghiên cứu về nguyên tố Iod
Iod được khám phá bởi Barnard Courtois vào năm 1811. Courtois là con trai của một nhà sản xuất Kali Nitrat, một chất được sử dụng trong thuốc súng. Trong quá trình sản xuất Kali Nitrat từ rong biển, Courtois phát hiện ra một chất khí màu tím. Ông nhận thấy chất khí này kết tinh thành tinh thể màu sẫm trên các bề mặt lạnh. Courtois đã chia sẻ mẫu tinh thể này với các nhà khoa học khác để tiếp tục nghiên cứu.

Lịch sử phát hiện và nghiên cứu về nguyên tố Iod
Charles Bernard Desormes và Nicolas Clément tiếp tục nghiên cứu với mẫu tinh thể của Courtois. Họ thông báo về phát hiện này vào ngày 29 tháng 11 năm 1813. Joseph Louis Gay-Lussac và André-Marie Ampère cũng được thông báo và tham gia nghiên cứu. Gay-Lussac đã đề xuất rằng mẫu vật có thể là một nguyên tố hóa học mới hoặc một hợp chất oxy. Ampère đã đưa mẫu vật cho Humphry Davy, người tiến hành thí nghiệm và nhận ra sự tương tự của iod với clo.
Xem thêm : Samsung Galaxy A73 5G (8GB | 128GB) Chính Hãng
Humphry Davy đã gửi thông điệp cho Hội Hoàng gia Luân Đôn vào ngày 10 tháng 12 để thông báo về việc phát hiện nguyên tố mới này. Một cuộc tranh cãi đã nổi lên về việc ai đã tìm ra iod trước tiên, nhưng cuối cùng Davy và Gay-Lussac đồng ý rằng Barnard Courtois là người đầu tiên đã phân lập nguyên tố iod này.
Trạng thái tự nhiên của Iod (I)
So với các halogen khác, iot có tồn tại rất ít trong vỏ trái đất. Điều này là do I-ốt thường bị hòa tan trong nước biển và không tạo thành khoáng chất phổ biến như các nguyên tố khác.

Trạng thái tự nhiên của Iod (I)
- Nước biển: Trong tự nhiên, iot được tìm thấy ở dạng hợp chất, chủ yếu là các muối Natri và Kali của nó. Nước biển là một nguồn chính của I-ốt, và nồng độ iot trong nước biển có thể dao động tùy thuộc vào khu vực địa lý.
- Rong biển: Một số loài rong biển có khả năng hấp thụ iot từ môi trường xung quanh. Do đó, I-ốt cũng có thể được tìm thấy trong một số hợp chất của rong biển.
- Tuyến giáp: Một sự xuất hiện đáng chú ý của I-ốt là trong tuyến giáp của con người. Tuy I-ốt chỉ có mức độ rất nhỏ trong tuyến giáp, nhưng nó lại rất quan trọng. Thiếu I-ốt có thể gây ra bệnh bướu cổ, một tình trạng mà tuyến giáp phát triển quá mức để cố gắng bù đắp sự thiếu hụt iot.
Các tính chất vật lý của I-ốt
Các tính chất vật lý của Iod là gì? Nó có các tính chất cơ bản như sau:

Các tính chất vật lý của I-ốt
- Trạng thái vật chất: I-ốt là một nguyên tố hóa học tồn tại dưới dạng chất rắn
- Màu sắc: I-ốt có màu tím đen khi ở dạng chất rắn
- Điểm nóng chảy: Điểm nóng chảy của I-ốt là khoảng 113,7 0C (236,7 0F). Ở nhiệt độ này, chất rắn I-ốt chuyển sang trạng thái lỏng.
- Điểm sôi: Điểm sôi của I-ốt là khoảng 184,3 0C (363,7 0F). Ở nhiệt độ này, chất lỏng I-ốt chuyển sang trạng thái hơi.
- Khối lượng riêng: Khối lượng của I-ốt là khoảng 4,93 g/cm3. Điều này có nghĩa là một khối lượng nhất định của I-ốt sẽ có thể chiếm một thể tích nhất định trong không gian.
- Hiện tượng thăng hoa: Khi đun nóng ở nhiệt độ cao, Iod không nóng chảy và chuyển thành hơi màu tím. Khi làm lạnh thì hơi Iod lại chuyển sang dạng tinh thể mà không chuyển qua trạng thái lỏng.
- Khả năng hòa tan: Iod ít hòa tan trong nước, nhưng nó lại tan rất nhiều trong các dung môi hữu cơ như: Benzen, xăng, rượu,…
Các tính chất hóa học của Iod là gì?
Iod (I) là một chất có tính oxi hóa mạnh, nhưng so với Clo hay Brom thì tính oxi hóa kém hơn. I-Ốt có khả năng phản ứng với các kim loại, khí Hidro, có tính oxi hóa và tính khử. Chi tiết như sau:

Các tính chất hóa học của Iod là gì?
Tác dụng với kim loại
Khi cho Iod (I) tác dụng với kim loại nó sẽ oxi hóa nhiều kim loại ở điều kiện nhiệt độ cao hoặc có chất xúc tác tham gia phản ứng.
2Al + 3I2 → 2AlI3
Tác dụng với khí Hidro
I-ốt hầu như không có tác dụng với nước, nhưng nó có thể oxi hóa khí Hidro ở điều kiện nhiệt độ cao và có chất xúc tác. Phản ứng hóa học sinh ra khí Hidro Iotua không bền. Đây là một phản ứng hóa học thuận nghịch.
H2 +I2 ↔ 2HI
Hidro Iotua lại là một chất có khả năng tan trong nước mạnh và nó tạo thành dung dịch axit Iothidric. Đây là một trong những axit mạnh, nó còn mạnh hơn cả axit HCl và HBr (HF < HCl < HBr < HI)
Tác dụng với Clo và Brom
Vì I-ốt có tính oxi hóa yếu hơn Clo và Brom, nếu trong phản ứng hóa học nó sẽ thế chỗ của Iod trong hợp chất.
Cl2 + 2NaI → 2NaCl + I2
Xem thêm : Nằm mơ thấy rụng nhiều răng có điềm báo gì? Giải mã các giấc mơ
Br2 + 2NaI → 2NaBr + I2
Tính khử của axit HI
HI là một axit có tính khử mạnh, nó có thể khử được axit H2SO4 đặc. Phương trình hóa học xảy ra như sau:
8HI + H2SO4 → 4I2 + H2S + 4H2O
2HI + 2FeCl3 → FeCl2 + I2 + 2HCl
Cách điều chế I-ốt
Iod (I) được điều chế như thế nào? Trong công nghiệp, người ta thực hiện điều chế I-ốt từ nguyên liệu rong biển. Ngoài ra, người ta còn thu Iod tinh khiết bằng phương pháp cho KI tác dụng với Đồng (II) Sunfat.

Cách điều chế I-ốt
Cũng có một số cách khác để tác Iod (I) ra khỏi hợp chất. Tạo bẹ cũng là một trong những loài thực vật có khả năng hấp thụ và tập trung khá nhiều I trong cơ thể. Nó mang Iod vào dây chuyền thức ăn tự nhiên và giúp cho việc điều chế Iod (I) có giá thành thấp hơn rất nhiều.
Để thu Iod (I) tinh khiết, người ta cho dung dịch NaI tác dụng với chất oxi hóa mạnh hơn, như Clo. Khi đó Clo sẽ đẩy I khỏi hợp chất NaI để thế chỗ nó.
2NaI + Cl2 → 2NaCl + I2
Các ứng dụng của Iod (I) hiện nay
Chi tiết về các ứng dụng của Iod (I) trong đời sống, sản xuất hiện nay như sau:

Các ứng dụng của Iod (I) hiện nay
- Dinh dưỡng: Iod là một nguyên tố vi lượng cần thiết cho sức khỏe con người. Thiếu Iod có thể dẫn đến các tác hại như bệnh bướu cổ và thiểu năng trí tuệ. Sử dụng muối Iod là một cách phòng ngừa hiệu quả cho tình trạng thiếu iod.
- Tuyến giáp: Iod là thành phần cần thiết để tạo ra Hormone tuyến giáp, Thyroxine và triiodothyronine. Những Hormone này đóng vai trò quan trọng trong quá trình điều chỉnh chức năng của cơ thể.
- Khử trùng: Dung dịch iod được sử dụng làm thuốc bôi để khử trùng vết thương và bề mặt chứa nước uống trong tủ thuốc gia đình.
- Ứng dụng hóa hữu cơ và y khoa: Hợp chất Iod có thể được sử dụng trong các ứng dụng hóa hữu cơ và y khoa như chất nhuộm, chất chống nhiễm khuẩn, và thuốc.
- Nhiếp ảnh: Muối Iodide bạc (AgI) được sử dụng trong quá trình chụp ảnh để tạo ra hạt bạc phản ứng với ánh sáng và tạo nên hình ảnh.
- Điều trị phóng xạ: Muối Iodide Kali (KI) có thể được sử dụng để điều trị bệnh nhân bị ảnh hưởng của phản ứng phân hạch hạt nhân, như rửa trôi đồng vị phóng xạ I-131 và Cs-137.
- Công nghệ đèn: Vonfram Iodide được sử dụng để làm ổn định dây tóc của bóng đèn đèn tóc.
- Y khoa hạt nhân: Iod-123 và Iod-131 được sử dụng trong y khoa để tạo ảnh và xét nghiệm hoạt động của tuyến giáp và điều trị các bệnh liên quan đến tuyến giáp.
- Tính độc: Iod nguyên chất có tính độc đối với tất cả các sinh vật.
Một số cảnh báo khi sử dụng Iod là gì?
Một số cảnh báo khi sử dụng Iod (I) mà các em cần biết như sau:

Một số cảnh báo khi sử dụng Iod là gì?
- Da tiếp xúc trực tiếp với Iod: Iod có thể gây tổn thương cho da nếu tiếp xúc trực tiếp trong thời gian dài. Do đó, khi làm việc với iod, cần đảm bảo sử dụng thiết bị bảo hộ như găng tay, áo choàng và kính bảo hộ để tránh tiếp xúc trực tiếp với da.
- Mắt và màng nhầy tiếp xúc với Iod: Hơi iod có thể gây khó chịu và kích thích mắt và màng nhầy. Nếu tiếp xúc với hơi iod, cần tiếp tục rửa mắt với nước sạch trong ít nhất 15 phút và tìm kiếm sự chăm sóc y tế nếu cần thiết.
- Mật độ Iod trong không khí cao: Mật độ Iod trong không khí nên được kiểm soát để đảm bảo an toàn. Trong một khoảng thời gian tiếp xúc kéo dài khoảng 8 giờ, mật độ Iod trong không khí không nên vượt quá 1 mm/m3, tính trung bình theo thời gian.
- Tuân thủ quy định an toàn: Khi làm việc với Iod, cần tuân thủ các quy định và hướng dẫn an toàn được thiết lập bởi các tổ chức và cơ quan liên quan. Điều này bao gồm việc sử dụng thiết bị bảo hộ cá nhân, lưu trữ và vận chuyển Iod theo quy định, và hạn chế tiếp xúc không cần thiết với nguyên tố này.
Như vậy, bài viết trên Admin đã tổng hợp và cung cấp mọi kiến thức quan trọng và có liên quan đến Iod. Với chia sẻ trong bài, các em không chỉ biết Iod là gì? Mà các em còn nắm rõ và hiểu đúng về I-ốt. Một nguyên tố quan trọng với cả con người và các sinh vật sống. Nhưng khi sử dụng chúng ta cũng cần biết một số cảnh báo để lưu ý. Theo dõi Admin để đón đọc nhiều bài viết chia sẻ bổ ích hơn nữa về các nguyên tố hóa học trong bảng tuần hoàn nhé!
Nguồn: https://duhochanquocchd.edu.vn
Danh mục: Khám Phá

/fptshop.com.vn/uploads/images/tin-tuc/179494/Originals/thanh-toan-cuoc-tra-sau-Viettel-7.jpg)
/fptshop.com.vn/uploads/images/tin-tuc/172854/Originals/etc-la-gi-5.jpg)










